Les molécules biologiques
Carl Richard Woese (1928 - 2012), en 1967, propose que la vie à son origine s´édifia sur la base unique de l´ARN, théorie reprise en 1986 par Walter Gilbert qui propose un monde ARN originel.
REMARQUE: la découverte, en 1982 de la fonction enzymatique de certains brins d´ARN (ribozymes) capables de catalyser des réactions chimiques, ajoutait une fonction à l´ARN qui déjà :
- portait l´information génétique,
- permettait de synthétiser les protéines
- pouvait s'autorépliquer,
- sans oublier les ARN interférents.
- les ribosomes.
- des réactions d'oxydo-réduction au cours desquelles un accepteur d´électrons (coenzyme NAD+) est réduit :
L´hypothèse d´un monde originel à ARN a aujourd´hui la faveur des scientifiques.
L´ARN se suffit donc à lui-même pour de multiples fonctions. D´où l´idée de faire de l´ARN le constituant primitif de la vie.
C´est donc en nous référant à un monde originel ARN que nous examinerons la création et l´évolution des molécules biochimiques.
Les molécules biochimiques
D´abord, constatons que, dans les océans, la concentration et la diversité des molécules nécessaires à la vie, n´atteignirent jamais celles de la soupe utilisée par les chercheurs dans leurs expériences.
Aussi pour retrouver des conditions capables de créer un début de vie élémentaire, on peut envisager que ce furent celles qui se réalisèrent il y a 3,6 milliard d´années dans une lagune.
On peut imaginer qu'il y a 4 milliards d'années, près du rivage d'un continent, l'océan chaud de quelque 90°C avait envahi le cratère créé il y a des millénaires par l'impact d'un gros astéroïde. Il s'y était formé une vaste étendue d'eau de quelque 50 kilomètres de diamètre et d'une profondeur de deux à trois cents mètres. L'ensemble bien isolé de l'océan possédait cependant des failles qui laissaient passer les plus hautes vagues. Cet apport, qui compensait les pertes par évaporation et fuites diverses, fut à l'origine d'une concentration d'éléments biochimiques qui, au fil du temps, devint de plus en plus importante.
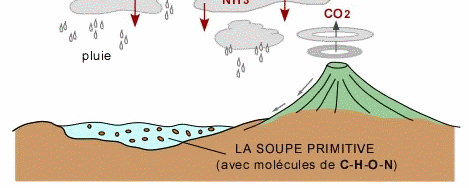
Divers lieux correspondaient, certainement, à cette description, mais il en fut au moins un présentant, un rapport entre évaporation et remplissage, plus favorable que les autre à une meilleure concentration d’éléments biochimiques. Cette lagune constituait une sorte de chaudron rempli de quelques (1012 m3) d'une soupe chaude (environ 90°) où, au terme d'un certain temps, les éléments créés précédemment s'y trouvaient concentrés, chacun à plusieurs milliards d'exemplaires par mètre cube.
Dans cette soupe primordiale, l'agitation thermique fut le seul catalyseur qui favorisa les assemblages des atomes et des molécules selon leurs affinités réciproques,
Exemple de liaisons chimiques prébiotiques
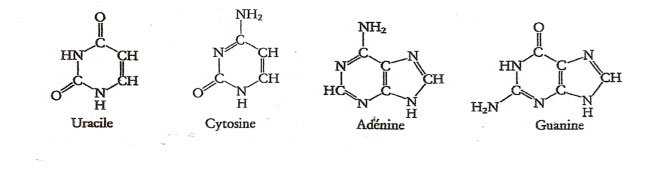
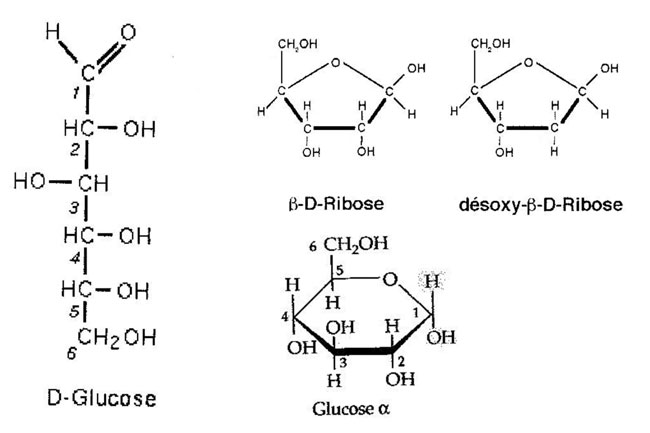
Des glucides : RIBOSE (C5H10O5), DESOXYRIBOSE (C5H1004), GLUCOSE (C6H1206).
Des acides aminés .
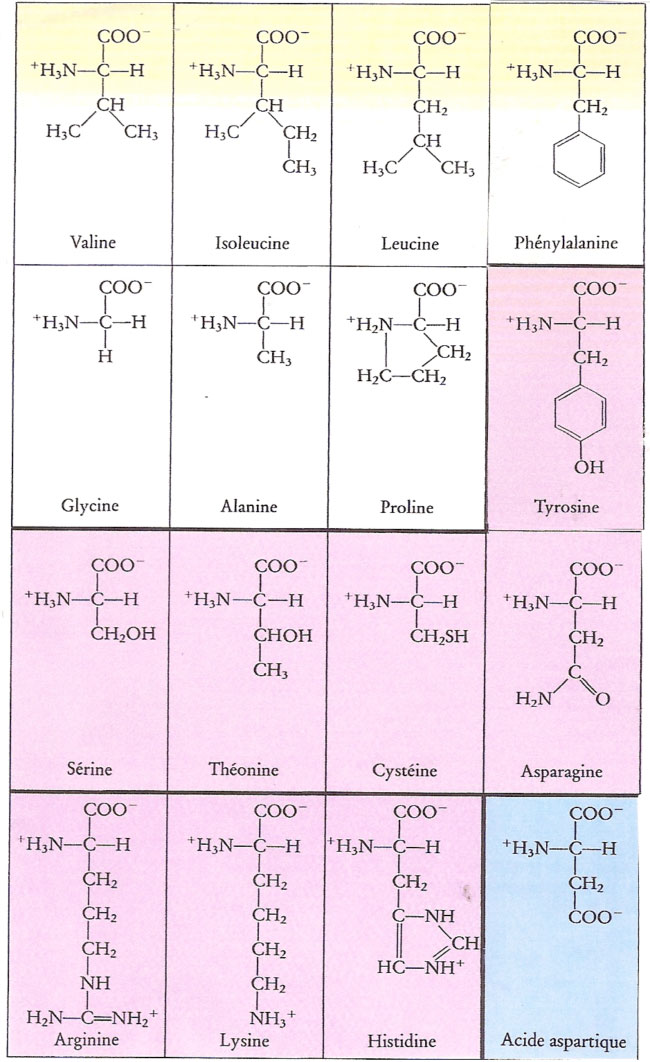
.4 - Les acides aminés sont les constituants des protéines.
Malheureusement il n´y avait aucune protéine dans la lagune et aucun moyen d´assembler des acides aminés pour en constituer.
Pour l´instant, seules les acides aminés sont présents dans la lagune. Cependant nous savons qu´une protéine est une macromolécule biologique composée d´une chaîne d´acides aminés liés entre eux par des liaisons peptidiques (chaîne polypeptidique). En général, on parle de protéine lorsque la chaîne contient au moins 100 acides aminés, et de peptide pour des assemblages de plus petite taille.
Les protéines sont des éléments essentiels de la vie de la cellule : elles peuvent jouer un rôle structurel (comme l´actine), un rôle dans la mobilité (comme la myosine), un rôle catalytique (les enzymes), un rôle de régulation de la compaction de l´ARN (les histones) ou d´expression des gènes (les facteurs de transcription), etc. En somme, l´immense majorité des fonctions cellulaires sont assurées par des protéines.
La structure des protéines est complexe et influe sur le rôle qu´elles jouent dans la vie de la cellule.
Malheureusement il n´y avait aucune protéine dans la lagune et aucun moyen d´en produire.
A titre d´information les protéines, enzymes, ont un rôle de catalyseur. C´est-à-dire qu´elles accélèrent une réaction chimique sans être elle-même consommée au cours de cette réaction.
Si une réaction chimique est possible, face à une protéine appropriée elle devient instantanée parfois même sélective. C´est-à-dire qu´elle ne se réalise que dans des circonstances particulières.
Tout cela reste vrai pour les protéines, mais qu´importe leur absence !
En effet, dans les années 1980, Tom Cech et Sidney Altman ont découvert que certains ARN, ensuite appelés ribozymes (de la contraction de ribose et enzyme), pouvaient avoir un rôle de catalyseur, comme les protéines. Cette découverte inattendue a valu à Cech et Altman le prix Nobel de chimie en 1989.
En 1990, Larry Gold et Jack Szostak ont mis au point une méthode visant à sélectionner les ARN montrant une activité catalytique.
Ils ont depuis réussi à identifier les chaînes d´ARN capables d´agir comme des protéines. Il s´agit des (ANRt) capables de se lier sélectivement à des acides aminés pour les transférer. Les ribosomes, ANRr, captables d´effectuer diverses fonctions lors de la traduction des protéines.
Les ribozyme ANRr et les ANRt (transfert) sont encore, aujourd´hui, sous leur forme primitive d´ARN.
5 -Les ATP:
Nous connaissions déjà l´adénine monophosphate l´AMP qui n´est autre que l´un des quatre nucl´otides.
L´adénosine-5'-triphosphate (ATP) est la molécule indispensable qui, dans la biochimie de tous les organismes vivants connus, fournit, en se dégradant, par hydrolyse l´énergie nécessaire aux réactions chimiques du métabolisme. C´est toute la différence avec une enzyme
L´ATP a été découvert en 1929 par Karl Lohmann, mais sa véritable structure a été découverte quelques années plus tard. Cette molécule a été synthétisée en laboratoire pour la premiére fois en 1948 par Alexander Robert Todd.
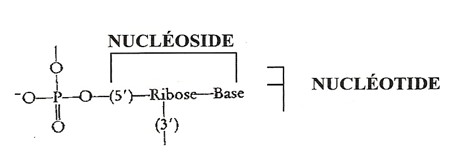
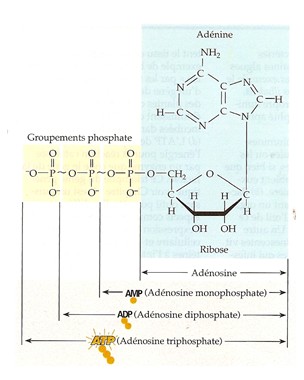 Si, à un nucléotide fait d´un adénine,
vous ajoutez un deuxième phosphate il devient un ADP ou adénosine diphosphate.
Si, à un nucléotide fait d´un adénine,
vous ajoutez un deuxième phosphate il devient un ADP ou adénosine diphosphate.
Si un troisième phosphate se joint à un ADP, celui-ci devient un ATP. Ce composé contient de l´énergie ; quand il se dégrade en ADP ou AMP, l´énergie libérée permet d´induire une réaction.
Les ATP, par hydrolyse, se transforment en ADT plus un phosphate (Pi) en restituant de l´énergie et vice versa, selon la formule :
ATP + H2 O →ADP + Pi + Energie (14 K CAL OU 58.600 J
Les ATP qui en donnant leur énergie perdent un phosphate ont l´occasion de le récupérer par divers processus comme la glycolyse
Ces ATP sont les ouvriers de la vie
Selon Christian de Duve, Prix Nobel de médecine en 1974 : la voie métabolique de la production d´énergie est celle quasi-universelle de la glycolyse, c´est-à-dire la dégradation du glucose en acide lactique avec dégagement d´énergie. Ce processus, dit-il, "porte la marque du primitif par sa relative simplicité". Il a comme cofacteur l´(ATP) peut être hydrolysé (coupé à l´aide d'eau) en (ADP) et phosphate inorganique (Pi) en produisant de l´énergie et inversement, par condensation de l´(ADN) et du (Pi) avec élimination d'eau et apport d´énergie, peut se reconstituer en (ATP) selon le processus de la glycolyse.
1 - ATP fournit de l´énergie (voir ci-dessus)
ATP + H2 O ←→ ADP + Pi + Energie (14 K CAL OU 58.600 J
2 - La glycolyse est un mécanisme de régénération d´ATP qui ne nécessite pas d´oxygène. Au cours de ce processus, on assiste à :

